- PDNレクチャーとは?
- Chapter1 PEG
- Chapter2 経腸栄養
- 1.経腸栄養の特徴と適応
- 2.経腸栄養剤の分類
- 3.病態別経腸栄養剤
- 3.1 病態別経腸栄養剤とは?
- 3.2 肝不全用栄養剤
- 3.3 腎不全用栄養剤
- 3.4 糖尿病用栄養剤
- 3.5 呼吸不全用栄養剤
- 3.6 免疫賦活栄養剤、免疫調節栄養剤
- 4.経腸栄養に用いられる製剤および食品
- 4.1 グルタミン製剤(食品)
- 4.2 微量元素製剤
- 4.3 食物繊維
- 4.4 プロバイオティクス、シンバイオティクス
- ① プロバイオティクス
- ② シンバイオティクス
- 4.5 ORS(経口補水液)
- 4.6 増粘剤、ゲル化剤
- 4.7 脂肪酸
- ① 脂肪酸とその分類
- ② 多価不飽和脂肪酸(ω-3, ω-6系)
- ③ 中鎖脂肪酸(MCT)
- 5.半固形化栄養剤
- 5.1 基礎的な知識
- 5.2 臨床的な知識
- ①胃瘻からの半固形化栄養材
短時間注入法 - ②栄養剤形状機能について
- 6.ミキサー食
- 6.1 ミキサー食(成人)
- 6.2 ミキサー食(小児)
- 6.3 ミキサー食(小児)
- 7.早期経腸栄養
- 8.周術期経腸栄養
- 9.在宅経腸栄養
- 9.1 在宅経腸栄養
- 9.2 在宅診療の医療費の実際
- 9.3 終末期医療にかかる費用
- 10.経腸栄養に必要な器具
- 11.経腸栄養時の薬剤投与
- 12.経腸栄養の管理
- 13.経腸栄養の合併症と対策
- 14.栄養剤使用時の栄養アセスメント
- ●「経腸栄養」関連製品一覧
- Chapter3 静脈栄養
- Chapter4 摂食・嚥下リハビリ
- PDNレクチャーご利用にあたって



Chapter2 経腸栄養
4.経腸栄養に用いられる製剤および食品
4.プロバイオティクス、
シンバイオティクス
①プロバイオティクス
戸塚共立第2病院 顧問
(前 昭和大学医学部外科学講座小児外科学部門 教授) 土岐彰

2025年3月版
1.プロバイオティクスの定義
プロバイオティクスは、抗生物質(antibiotics)に対比する言葉で、その起源は、生物間の共生関係(probiosis)を意味する。
プロバイオティクスは、腸管内の善玉菌を増やして腸内細菌のバランスを保ち、健康な体を作ることを目的としており、1989年に「腸内細菌のバランスを改善することにより、宿主に有益な作用をもたらす生きた微生物」と定義されたが1)、1992年になって、「1種類または混合培養の細菌で、動物やヒトに投与されると内在性細菌叢の性質を改善することにより、宿主に好影響を与えるもの」との案も出された。さらに、1998年に「適正な量を摂取したときに、宿主に有用な作用を示す生菌体」と定義され、現在広く使われている。
2.プロバイオティクスの原理(善玉菌と悪玉菌)
腸管内には数100種類、100兆個もの細菌がすみついている。この腸管内には、乳酸菌やビフィズス菌に代表される健康に良い善玉菌と、腐敗や発ガン関連物質を生み出すウェルシュ菌に代表される健康に有害な悪玉菌が存在する。これら2種類の細菌バランスが人間の健康状態を左右している。
悪玉菌が増えると有害物質・ガスをつくり、それが体内に吸収され、肝機能障害、便秘、下痢などの原因となる。それが長期にわたると、免疫力が低下し、病原菌へ感染する可能性が増え、発ガン物質の生産を促す。いったん減少した善玉菌を腸管内で増加させることは難しい。そこで外部の善玉菌を送り込む方法がとられ、これがプロバイオティクスである。
善玉菌の代表としての乳酸菌は、グラム陽性菌でカタラーゼ陰性、芽胞形成(-)、酸素の少ない環境を好み、ブドウ糖を発酵して50%以上の乳酸を生成する細菌である。一方、ビフィズス菌は、F-6-リン酸経路を介してブドウ糖から酢酸とL型乳酸を生成する。
プロバイオティクスとして用いられている乳酸菌およびビフィズス菌を表1に示す2)。
|
Strain |
Source |
|---|---|
|
Lactobacillus acidophilusNCFM |
ダニスコ(デンマーク) |
|
Lactobacillus acidophilus SBT-2062 |
雪印乳業 |
|
Lactobacillus acidophilus R 0052 |
インスティチュート・ |
|
Lactobacillus acidophilus LA-1 |
クリスチャンハンセン |
|
Lactobacillus casei Shirota |
ヤクルト |
|
Lactobacillus casei lmmunitas |
ダノン(フランス) |
|
Lactobacillus fermentum RC-14 |
ユーレックスバイオテック(London,Ontario,Canada) |
|
Lactobacillus johnsonii Lj-1 |
ネスレ(スイス) |
|
Lactobacillus plantarum 299 V |
プロビAB(スウェーデン) |
|
Lactobacillus reuteri SD 2112 |
バイオガイア(Raleigh,NC) |
|
Lactobacillus rhamnosus GG |
バリオ(フィンランド) |
|
Lactobacillus rhamnosus LB 21 |
Essum AB(スウェーデン) |
|
Lactobacillus salivarius UCC 118 |
University College |
|
Bifidobacterium longum BB 536 |
森永乳業 |
|
Bifidobacterium lactis HN 019(DR 10) |
フォンテラ |
|
Lactobacillus acidophilus LB |
Lacteol Laboratory |
|
Lactobacillus paracasei F 19 |
Medipharm |
3.腸内細菌叢の推移
通常、腸内細菌叢は、生後の細菌パターンと菌数などから3群に分類される。Ⅰ群は、生後やや遅れて出現する最優勢菌数の菌群で、長い歴史の中で宿主と共生関係を築いたと考えられる。プロバイオティクスに用いられるビフィズス菌や無毒性バクテロイデス、eubacterium などがこれにあたる。生後1週間目にはビフィズス菌が全体の90%以上を占めるようになる3)。(図1)Ⅱ群は、生後まもなく出現し、一時最優勢となるが、まもなくⅠ群と交代して減少し、以降中等度の菌数を維持する菌群である。Ⅰ群同様にプロバイオティクスに用いられる。乳酸菌のほかに無毒性大腸菌、ブドウ球菌がこれに含まれる。Ⅲ群は、少数で多くは病原性があり、宿主の防御機構を破壊して、日和見感染をおこす菌群である。Clostridium perfringens、毒性バクテロイデス、緑膿菌、毒性大腸菌、黄色ブドウ球菌などがこれに含まれる。いったん確立した腸内細菌の構成は、ほぼ安定しているが、徐々に成人パターンへと変化する。老齢になるとビフィズス菌は減少するが、バクテロイデス、eubacterium、ウェルシュ菌などが増加し、腸内環境は悪化していく4)。
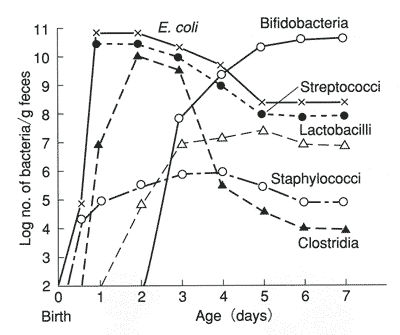
4.病態における腸内細菌叢
腸内常在細菌は、宿主との間で一定の平衡状態を保ちつつ、互いに共存しており、通常は無害である。宿主側に何らかの不均衡が生ずると、病原性細菌が増殖し、病原性を発揮する。いわゆる「日和見感染」である。
5.プロバイオティックスの効果
乳酸菌やビフィズス菌は整腸作用の他に、免疫機能を高め、がんや感染症を予防し、免疫機能を正常化してアレルギー体質を改善したり、さらには動脈硬化などの生活習慣病を予防する働きがある。
また、花粉症の軽減効果も注目されている。これは、ビフィズス菌摂取により、Th1細胞が活性化され、Th2細胞が抑えられたため、花粉症に敏感に反応する抗体が作られなくなって症状が軽減されたものと考えられている5)。
プロバイオティクスの主な効果を以下に示す。
- 腸内細菌叢の正常化
- 便秘・下痢の改善(整腸作用)
- 感染予防
- 血圧降下作用
- コレステロール低下
- アレルギー症状改善
- 免疫システムの賦活化
- 腫瘍抑制効果
- 発ガンプロモータの抑制
6.プロバイオティクスの臨床応用
プロバイオティクスが臨床的に応用されている主な疾患を以下に示す6)。
① 胃腸炎・急性下痢症(感染性腸炎)
感染性腸炎に関しては、下痢の持続時間の短縮、下痢の4 日以上の持続性の低下、発症2日目の下痢回数の減少において統計学的に有意な効果を示している。
② 抗菌薬誘導下痢症(Antibiotic Associated Diarrhea:AAD)・Clostridium difficile感染症(Clostridium
difficile Infection:CDI)
抗菌化学療法を施行された患者の約20%にAAD
を発症するリスクがある。抗菌薬単独投与患者の腸内細菌叢は、偏性嫌気性菌の顕著な減少およびBifidobacteriumの検出率の有意な低下を認め、59%の患者が腹部症状を訴えた。一方、抗菌薬投与開始3日目からミヤBMⓇを併用した場合は、腹部症状発症率が5%まで低下し、抗菌薬投与開始と同時に併用した場合は、9%まで低下した。このことは、プロバイオティクスの臨床的有効性を示している。
③ 炎症性腸疾患(Inflammatory Bowel Disease:IBD)
IBDは、消化管粘膜の慢性炎症または潰瘍を引き起こす疾患で、消化管全体に病変が広がるクローン病と主に大腸に病変が限局する潰瘍性大腸炎がある。腸内細菌叢の異常が病態の発症、増悪、再燃に密接に関与することが明らかとなり、制御性T細胞を誘導する腸内細菌による疾患制御の可能性が期待されている7,8)。
④ アレルギー性疾患(アトピー性皮膚炎など)
妊婦へのプロバイオティクス投与により、新生児のアトピー性疾患発症を予防する可能性が示唆されている。9)
7.プロバイオティクスと短鎖脂肪酸
腸内細菌は食物繊維、オリゴ糖などの難消化性糖質を嫌気的に代謝(発酵)して、短鎖脂肪酸、水素、二酸化炭素、メタンに分解する。短鎖脂肪酸は、酢酸、プロピオン酸、酪酸で炭素数1~6の脂肪酸である。通常、代謝された糖質エネルギーの約60%が短鎖脂肪酸に変換される。
この短鎖脂肪酸は腸管粘膜細胞、とくに結腸粘膜細胞そのもののエネルギー源であり、そのことが結腸粘膜増殖を促進する。また、短鎖脂肪酸は消化管内のpHを下げ、これが結腸粘膜を増殖させる。DNA合成、蛋白合成およびすべての酵素反応はpHに依存しており、細胞外液pHが下がると細胞内液pHも下がり、細胞分裂が活発化して、結腸粘膜が増殖するといわれている。また、胆汁酸代謝はpHに依存しており、pH6.5以下になると、この代謝の第一段階である7α-dehydroxylationが完全に抑制され、chenodeoxycholic acidのような強い粘膜増殖作用をもつ胆汁酸が消化管内に蓄積する。
一方、消化管内の短鎖脂肪酸は、それ自体腸管の血流を増加し、腸管順応を促すといわれている。また、すべての腸腺窩細胞の増殖速度は血漿中enteroglucagon濃度に関係している。すなわちenteroglucagonは腸管細胞新生を促進する作用がある。また、enteroglucagon分泌細胞は回腸末端および結腸に存在し、短鎖脂肪酸とくに酪酸が、直接あるいは間接的にenteroglucagon分泌を刺激しているといわれている。
さらに、空腸粘膜増殖機序は、短鎖脂肪酸の刺激が自律神経を介して結腸からcentral nerve systemへ伝達されることにより作られる二次的な神経伝達物質やホルモンによるといわれている。これらが腸管上皮細胞や肝臓を刺激し、gastrin やgrowth factor を分泌させ、小腸とくに空腸のそれぞれのレセプターを介して粘膜増殖を促進している10)。
8.プレバイオティクス(Prebiotics)
プレバイオティクスとは、「腸内の有用微生物の増殖促進、または有害微生物の増殖抑制によって宿主の健康に有利に役立つ難消化性食物成分」と定義されている11)。この有用微生物として、ビフィズス菌と乳酸菌があり、難消化性オリゴ糖から乳酸や酢酸を産生し、最終的に短鎖脂肪酸が生成される。これらの短鎖脂肪酸は腸内pHを低下させることで有害微生物の増殖を防いでいる。また、ビフィズス菌や乳酸菌などの善玉菌を腸管内で増加させて腸内細菌叢を改善させる。難消化性オリゴ糖は、ビフィズス菌の好物で、これを摂取すると、腸内のビフィズス菌が活発になる.すなわち腸内細菌の食事と考えればよい。また、この「オリゴ糖」は悪玉菌の食事としては利用されない。
9.シンバイオティクス(Synbiotics)
シンバイオティクスとは、プロバイオティクスとプレバイオティクスを両方併せ持つもので、例えば、ビフィズス菌とオリゴ糖を同時に摂取することを意味する。
文献
- Fuller R: Probiotics in man and animals. J Appl Bacteriol 66: 365-378, 1989
- 外岡俊樹、ほか:プロバイオティクス、シンバイオティクスとは ―プロバイオティクスの保健機能を中心に―. 小児内科 39: 1160-1165, 2007
- 光岡知足: ヒトの健康における腸内フローラの役割. 光岡知足編: 腸内フローラの生態と役割, 学会出版センター, 東京, P4, 1990
- 永田 智: 小児領域におけるプロバイオティクス治療. 順天堂医学 51(4): 509-518, 2005
- Xiao JZ, et al: Probiotics in the treatment of Japanese ceder pollinosis: a double-blind placebo-controlled traila. Clin Exp Allergy 36: 1425-1435, 2006
- 高橋志達: プロバイオティクス、臨床応用への新しい方向性. 日本化学療法学会雑誌 66(4): 489-503, 2018
- Hayashi A, et al: A single strain of Clostridium butyricum induces intestinal IL-10-producing macrophages to suppress acute experimental colitis in mice. Cell Host Microbe 13: 711-722, 2013
- Kashiwagi I, et al: Smad2 and Smad3 Inversely Regulate TGF-β Autoinduction in Clostridium butyricum -Activated Dendritic Cells. Immunity 43: 65-79, 2015
- Kalliomäki M, et al: Probiotics in primary prevention of atopic disease: a randomized placebo-controlled trial. Lancet 357: 1076-1079, 2001
- 土岐 彰、ほか: 経腸栄養における食物繊維の意義. 小児外科31: 678-683, 1999
- Gibson GR, et al: Dietary modulation of the human colonic microbiota: introducing the concept of prebiotics. J Nutr 125: 1401-1412, 1995
関連製品情報
経腸栄養に用いられる製剤・食品



