- PDNレクチャーとは?
- Chapter1 PEG
- Chapter2 経腸栄養
- Chapter3 静脈栄養
- 1.末梢静脈栄養法(PPN)
- 1.1 PPNの特徴と適応
- 1.2 PPN製剤の種類と適応
- 1.3 PPNカテーテルの種類
- 1.4 PPNカテーテルの留置と管理
- 2.中心静脈栄養法(TPN)
- 2.1 TPNの特徴と適応
- 2.2 CVカテーテルの種類
- 2.3 CVカテーテル留置法
- 2.4 皮下埋め込み式CVポートと
その留置法 - 2.5 PICCとその留置法
- 2.6 エコーガイド下での
CVカテーテル留置法 - 2.7 TPN時の使用機材
- 2.8 TPN基本液とキット製剤の種類と特徴
- 2.9 アミノ酸製剤の種類と特徴
- 2.10 脂肪乳剤の種類と特徴
- 2.11 TPN用ビタミン製剤の種類と特徴
- 2.12 微量元素製剤の種類と特徴
- 2.13 TPNの実際の投与方法と管理
- 2.14 TPNの合併症
- 2.15 特殊病態下のTPN
- 2.16 小児のTPN
- 2.17 TPN輸液の調製方法
- 2.18 HPN(在宅経静脈栄養)
- Chapter4 摂食・嚥下リハビリ
- PDNレクチャーご利用にあたって




2025年3月版
<Pitfall>
TPN液は時間をかけて投与される。調製時に微生物が混入すると時間経過とともに微生物が増殖する可能性がある。TPNを調製する際には、
① 手指の消毒、② 調製環境の整備、③ 調製者の無菌調製を行う
という意識が大切になる。
1.はじめに
高カロリー輸液製剤は様々なキット製剤が発売されている。キット製剤は細菌汚染や異物混入のリスクが少なく、調製の手間も省けるため有用性の高い製品である。しかし、キット製剤が適応とならないケースも多くある。たとえば腎不全の患者に必須アミノ酸の多いアミノ酸製剤(キドミン®、ネオアミュー®)を使用したり、心不全の患者で水分や電解質を調製したりする場合である。もちろん新生児や小児のTPN(total parenteral nutrition)組成も成人とは異なるため、キット製剤は適応にならない。NST(nutrition support team)活動が全国的に展開されるようになった。様々な職種で個々の患者に最適な輸液組成を考えている。その場合キット製剤のアミノ酸量では不足していたり、電解質やビタミン量の細かい調節が迫られる症例もある。清潔で簡便なキット製剤が適応できればそれに越したことはない。しかし特殊な処方例となるケースも多く、その調製方法を知ることも重要である。本稿ではTPN輸液の調製時の留意点について述べる。
2.調製からTPN投与が終了するまでの時間
TPN輸液は、薬液を吸い上げた後にワンショットで静注するのと比較し、調製してから約一日かけて投与することになる。時間経過と共に輸液中で細菌や真菌などの微生物が増殖してしまう可能性があり、輸液調製時の汚染防止に留意する必要がある。白石先生らは、輸液が汚染された場合、約6時間経過後に大腸菌やセラチアといった細菌が爆発的に増殖したことを報告している1)。この6時間の意味合いとは、微生物側からみると、薬液中のアミノ酸などが栄養源となるかどうか、栄養源ならどうやって食べるかを検討している時間である。6時間位掛けて栄養源になるとわかると輸液中で一気に増殖する。細菌や真菌といった微生物はアミノ酸液や脂肪乳剤で増殖することがわかっている。微生物の栄養源となり得るTPN輸液を調製する際、目には見えないこれらの異物を混入させない努力すなわち無菌操作を行う必要がある。
3.調製者の問題
医療施設においてTPNは、無菌的に調製することが望まれる。無菌的にTPNを調製するために、CDC(米国疾病予防管理センター)のガイドラインでは、薬剤混合は薬剤部内において行うべきであるとされている。また日本病院薬剤師会のガイドラインでは、注射薬調剤の衛生管理に関する最終的な責任は薬剤師が行い、作業手順については薬剤師が監督指導を行うこと、としている2)。ではすべての病院あるいは医療施設において薬剤部で無菌調製を行っているだろうか? 答えはNoと言わざるを得ない。井上先生が2004年に調査したデータでは、薬剤部で調製が行われていたのは、約40%であったことが報告されている3)。TPN液は薬剤部で混合調製するべきである、と書いたが、薬剤師がクリーンベンチで混合調製した場合、必ず無菌といって良いだろうか?
この答えもNoである。TPNを無菌的に調製するためには、調製する個々人が無菌調製の意義を知り、様々な点に注意して無菌調製を行う姿勢が大切だと考える。筆者は以前、クリーンベンチで調製したTPN液の無菌試験を行なった。調製に不慣れな新人薬剤師ではクリーンベンチで調製しても細菌が検出され、調製に慣れたベテランの薬剤師では細菌が検出されなかったことを経験した。無菌操作では、薬液を吸いあげる針先は絶対に他のものに触れてはいけない。触れたか触れないかは調製者自身にしかわからない。針先が手袋などに触れたと思ったら、その針は廃棄しなければならない。 「薬液を汚染させてしまった」と思ったら、薬液自体も廃棄する、といった姿勢が大切である。筆者らが行った新人とベテラン薬剤師の無菌試験の結果は、調製者の注意力、無菌調製に対する意識の差が、異なった結果の得られた要因であると考えている。
4.TPNの調製環境
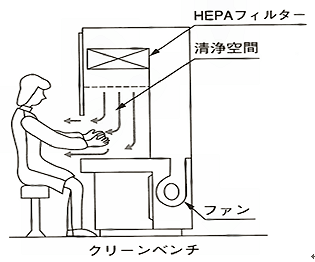
クリーンベンチの空気の流れを図に示す(図1)。クリーンベンチ上部から流れ出る空気はHEPA ( High Efficiency Particulate Air)フィルターという「篩い」に掛けられ、微粒子が除去された空気が排出される(手術室の環境と似ている)。クリーンベンチ内の清浄度は、一立方あたりの0.1μm以下の微粒子数が100個以下(クラス100)と決められている清潔な空間である。
ただし注意すべき点は、クリーンルーム中の浮遊微粒子はゼロではないことである。クリーンベンチで薬液を混合するときには、なるべくクリーンベンチの奥の方で薬液を混合する必要がある。フードの手前から15cm以上は奥で調製することが推奨されている。一方、通常環境の浮遊微粒子は計り知れないほど多いと考えられる。通常のオフィスの環境では、クラス 1,000,000 以上の値といわれている。クリーンベンチで薬液を混合した場合、まったく細菌が検出されなかったのに対して、病棟で混合した場合は15%程度に細菌が検出されたことも報告されている4)。
では病棟で薬液を混合する場合はどのように考えればよいか? 調製者は必ず手指消毒を行い、調製する場所は他の業務とは隔てた区域で行うことが大切だと言われている。薬剤部での混合調製が100%ではない現状では、このような調製環境を整えることが重要である。つまり薬液の汚染源は、「人の手」や「人の動き」だということを意識することである。手を清潔にして余計な動作を行わない、薬液を混合調製している時には他の人は立ち入らない、といったことが余計な粉塵を舞い上がらせないために必要な措置である。もちろん「会話」も厳禁である。これはクリーンベンチ内で操作を行なっている場合も同様である。保土田先生らの報告では、クリーンベンチで調製を行なっているときに人が動いただけで多くの微粒子が検出されたことが報告されている5)。
また最近、在宅でTPN液が使用されるケースが増えている。薬液の混合を在宅で行わなければならない場面も想定される。この場合、在宅で清潔な環境を整えるために、出来るだけ湿気(多くの微生物は湿気を好む)が少なく、埃の少ない部屋や服装を選んで調製することが望ましいとされている。
調製時の服装としては、素肌を出さないように袖口が詰まる白衣を着て手袋を着け、マスク、帽子をかぶることが望まれる。また調製する作業台はアルコール綿又はアルコール含有清拭用クロス(消毒用エタノール又は50~70%イソプロパノール)で清拭する必要がある。
さらに高齢社会の到来に合わせ、在宅医療が急激に進展している。薬局において在宅患者に対する無菌製剤(注射薬)の調剤も増加してきている。薬局で無菌調製に取り組む場合については、日本薬剤師会が中心となってまとめた資料にその考え方が示されている6)。 またこの考え方の基となっているものにASHPや日本病院薬剤師会などが示した「高カロリー輸液の調製に関するガイドラインの策定」がある。この中で強調されている点は無菌調製した製剤を冷所保存するのか否か、調製後28時間を超えて投与するのか、0.2μmのフィルターを使用して投与するのか、といった点などにおいて汚染のリスクを分類している点である7)。これらの考え方に基づいて出来うる限りクリーンベンチを使用するなど様々な点に配慮して栄養剤を無菌的に調製する必要がある。
5.医薬品の外包装
薬液は段ボール箱で病院に搬送されている。したがって医薬品の外包装は汚染されていると考えられる。だからといって外包装の消毒は必要だろうか? 答えはNoである。アルコールで浸漬すればそのアルコールは効果を失う。アルコールを交換する必要がある。これでは大変なコストがかかってしまう。クリーンベンチに薬液を持ち込む場合、外包装をアルコールで噴霧する。外包装があまりに汚れている、例えば病棟から返却された薬液を調製しなければならない時などに限って洗浄する、と考えれば良い。先ほど、手袋を着けて調製すると書いたが、外包装を触った手袋は汚染される。薬液を吸い取った針先などが手袋に触れてはいけない。
① ゴム栓
輸液のボトルキャップやアミノ酸製剤のシールを取ると、薬液を混注するゴム栓部分となる。輸液メーカはゴム栓部分の無菌性は保証していない。ゴム栓部分は必ずアルコールで消毒する。2種類以上の薬液を輸液本体に注入する際、薬液を混注する「回数」を減らすことも汚染対策として重要である。
② コアリング
ゴム栓に針を刺して薬液を混注する際には、針はまっすぐ刺す。斜めに針を刺すと、「コアリング」といって、ゴム栓部分を削りとってしまう場合がある。2種類以上の薬液を輸液の本体に混注する際には、ゴム栓の違う部分から混注することもコアリング対策として大切である。
6.アルコール(70%エタノール液)による消毒
アルコールは必ずしも万能な消毒薬ではない。例えば通常、何百℃といった高温で「ご飯」を炊く。お釜の中は無菌であろうか? お釜の中のご飯を放っておくと黄色くなる。これはバチルスという細菌が生き残っていて繁殖するためとも言われている。とてもしぶとい細菌でアルコールでも退治できない。またセラチアという細菌もアルコールに抵抗性を示す。実際、これらの細菌によって血流感染が生じてしまったケースも報告されている2)。「アルコールで拭いたから大丈夫」ではない。細菌がゴム栓に付いたり、薬液に入らないようにするために、前述した調製環境や調製者の服装や手技、意識が大切である。またガーゼカストに入れたアルコールは、ガーゼカストを開けた瞬間にアルコールの臭いがする。アルコールが揮発しているのである。ガーゼカストの蓋はなるべく閉じておくことが必要で、何日も同じガーゼカストを使うのも考えものである。単包化されたアルコールを使えば、アルコールが揮発するといったリスクを減らすことができる(図2)。
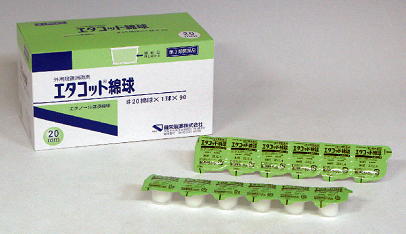
7.アンプルの扱い
日本ではアンプルの注射薬が数多く発売されている。アンプルを割る前には必ずアルコールでカット部分を消毒する8)。ところでアンプル薬品の製造工程では、最終的にアンプルを封入するときに熱をかけてアンプルを封印する。つまりアンプル内は陰圧である。色々なものを吸い込みやすくなっている。アンプルを割るとガラス片が飛び散るが、ガラス片はアンプル内に入ってしまう。したがってアンプルを割ったら10秒くらいは静置してガラス片を沈めこませる9)。60秒くらい静置した方が良いとする報告もある。アンプルから薬液を吸い取る時にはガラス片を吸い取らないように出来るだけ上澄みを吸い取るのが良く、アンプルを傾けてアンプルの肩口から薬液を吸い取るようにする。また開封したアンプルの上を、手が通っただけで微粒子がアンプル内に落下してしまう。開封したアンプルはなるべくクリーンベンチの奥に置くのが良い。このようにアンプル製剤の混合時は汚染する機会が増えるため、混合する薬液は最小化することが必要である。アンプル製剤はガラスアンプルに代わって、プラスチックアンプル製剤が発売されるようになった。プラスチックアンプル製剤はガラス片が飛び散らず、安全に使用できる可能性がある。それよりももっと進化したのが、プレフィルドシリンジである(図3)。プレフィルドシリンジは、TPNに混注することの多い総合ビタミン剤や微量元素製剤、補正用電解質液などの製品が発売されている。業務の効率化や異物混入、感染防止に役立っている。ただしプレフィルドシリンジは高価である。クリーンベンチ内で薬液を混合するといった施設では不要と思われるので、費用対効果を勘案して導入するのが良い。
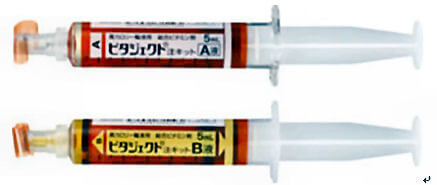
8.配合変化
去痰剤であるブロムヘキシン(ビソルボン®)は酸性の注射薬である。ここにアルカリ性のたとえばフロセミド(ラシックス®)を同じシリンジに吸い取ると白濁してしまう。酸とアルカリが反応して「塩」が出来たためである。このケースの外観変化はすぐに起る。しかし、中には輸液を開始して数時間経過した後に点滴ルートが白濁していたり、薬液中に白濁した沈殿物がみられるケースもある。このような場合、フィルターが目詰まりを起こしてしまう。
万が一、配合変化で生じた沈殿物が体内に投与されると、例えば新生児では血管が細いため肺動脈にそれが詰まってしまい不幸な転帰を辿ったというケースも報告されている。配合変化は輸液中のpHや温度などで反応が促進したり遅延したりする。時間をかけて投与するTPN液だから、投与が終了するまでに配合変化が起きる薬品の組み合わせでないか、混合する薬液の処方をチェックする必要がある。また輸液中に異物がないか、薬液を調製した後や患者さんに投与している最中にも薬液中やラインに異物がないか確認する必要がある。脂肪乳剤は白色の液体だが、脂肪乳剤に他の薬液を混合した場合、沈殿物が生じてもそれを確認することができない。したがって脂肪乳剤は単独に使用する必要がある。
TPN液の調製で最も困るのがリン酸イオンとカルシウムイオンは同時に配合できないことである。両者を混合するとリン酸カルシウムという塩ができて沈殿してしまう。市販のTPNキット製品では、塩酸を加えて酸性化してあったり、グリセロリン酸やクエン酸を加えることで両者が沈殿しない工夫が凝らされている。特殊な組成を自前で調製する場合、溶解度積といって少量であれば両者の混合は可能だが、これらの要求量の高い新生児や小児では十分量を投与することが困難となるケースもある。この場合、両者を朝と夕の交互に投与することや別のルートで投与するといった方法が必要になる。一方、目に見えない配合変化が起こるケースもある。アミノ酸製剤には酸化防止剤として亜硫酸ナトリウムが加えられている。亜硫酸ナトリウムはビタミンB1を分解してしまう。この変化は目で確認することができない。このためビタミン剤は投与直前に混注することが望ましい。また、光で分解しやすいビタミンも多くTPN液では遮光袋を掛けることも必要である。
9.ファイナルフィルター
フィルターは文字通り、ろ過をさせる器材である。細菌の大きさは最も小さい緑膿菌でも0.22μm程度と言われている。ファイナルフィルターの大きさはこれ以下なので、細菌や真菌をろ過する(通過させない)ことが可能である。CDCでは静脈栄養時にファイナルフィルターをつけることを推奨していない。しかしアメリカと日本では薬液の調製環境が異なっていたり、本邦ではガラスアンプルが多いといったように両国における様々な条件が異なる。TPNキット製剤を使って何も加えないといった場合を除いて、TPN液を投与するときにはファイナルフィルターを組み込む必要がある10)。ただし仮性菌糸を伸ばして増殖するCandida albicans は非対称膜のフィルターを貫通することが報告された11)。したがってTPNの場合には対称膜で構成されたフィルターを用いるべきである。
10.その他のTPN用器材
上記以外のTPN用の医療器材には、高カロリー輸液用の空のバッグ(600ml~3,000ml)やバッグ製剤とバッグ製剤の混合に用いられる連結管、メンブランフィルターといってシリンジと針の間につけるフィルターなどがある。特にメンブランフィルターは試薬から調製するセレンなどを調製した時に装着する必要がある。
11.おわりに
以上、TPN輸液の調製方法について述べた。TPN液は微生物汚染の温床になる。そのことを常に意識して薬液を調製することが肝要で、在宅でTPN液を施行される患者や家族にも適切に指導し実施して頂くことが望まれる。
さらに本当にTPNの適応があるのか、との吟味が必要であることは論をまたない。
文献
- 白石正、他:環境感染 22:165-169,2007
- 中西弘和、他:日本病院薬剤師会雑誌 41:1025-1027,2005
- 井上善文、他:静脈経腸栄養 19:37-48,2004
- 豊口義夫、他:Pharmacy Today 4:27-33, 1991
- 保土田誠一郎、他:薬学雑誌 119:921-928 1999
- 薬局における無菌製剤(注射剤)の調製について平成24年8月23日 日本薬剤師会
- 鍋島俊隆、他:日本病院薬剤師会雑誌 40: 1029-2037,2004
- 河崎陽一、他:日本病院薬剤師会雑誌 43:1198-1201 2007
- 河崎陽一、他:日本病院薬剤師会雑誌 43:927-930 2007
- 井上善文 :静脈経腸栄養 24:1163-1167 (2009)
- 井上善文:外科・代謝栄養 42:11-18(2008)



